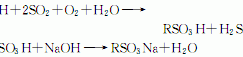结构式
| 物竞编号 | 01J6 |
|---|---|
| 分子式 | CaC2 |
| 分子量 | 64.10 |
| 标签 |
电石四级, 电石, Calcium acetylide, Acetylenogen, 其它 |
编号系统
CAS号:75-20-7
MDL号:MFCD00010905
EINECS号:200-848-3
RTECS号:暂无
BRN号:3909011
PubChem号:24856368
物性数据
1.性状:无色晶体,工业品为灰黑色块状物,断面为紫色或灰色。[1]
2.熔点(℃):2300[2]
3.沸点(℃):分解[3]
4.相对密度(水=1):2.22[4]
5.辛醇/水分配系数:-0.30[5]
6.引燃温度(℃):>325[6]
7.溶解性:暂无资料
毒理学数据
1.急性毒性 暂无资料
2.刺激性 暂无资料
生态学数据
1.生态毒性 暂无资料
2.生物降解性 暂无资料
3.非生物降解性 暂无资料
4.其他有害作用[7] 该物质对环境有危害,应特别注意对水体的污染。
分子结构数据
暂无
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:5
4.可旋转化学键数量:8
5.互变异构体数量:无
6.拓扑分子极性表面积61.8
7.重原子数量:18
8.表面电荷:0
9.复杂度:271
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:1
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
1.稳定性[8] 稳定
2.禁配物[9] 水、醇类、酸类
3.避免接触的条件[10] 潮湿空气
4.聚合危害[11] 不聚合
贮存方法
储存注意事项[12] 储存于阴凉、干燥、通风良好的专用库房内,库温不超过32℃,相对湿度不超过75%。远离火种、热源。包装必须密封,切勿受潮。应与酸类、醇类等分开存放,切忌混储。储区应备有合适的材料收容泄漏物。
合成方法
1.电炉还原法是目前工业上生产碳化钙的唯一方法。这种方法早在1895年美国实现工业化生产,生产中高温操作、粉尘较多、电能消耗大,工艺的改进可使操作条件改善、减少散热损失和提高一氧化碳回收利用率,多采用密闭式和大型化电石炉。将焦炭和石灰粉碎,按配比混合均匀加入密闭式电石炉,通电加热,在2000-2200℃下进行还原反应,生成熔融电石,自炉内流入电石锅冷却、破碎、包装。公斤/吨焦炭(固定炭84%) 550石灰石(CaO92%) 840电极糊 30电 3200(度/吨)
2.碳化钙可由碳和金属钙两元素在电弧炉中直接合成,或者用氧化钙和碳在电弧炉中2000℃高温反应制得,由这两种方法制得的产品纯度都不高。用氰氨基化钙CaCN2或氰氨基化钙与碳在高真空中加热制得碳化钙纯度可达99%。
在氧化铝舟中装有纯的氰氨基化钙或氰氨基化钙与乙炔炭黑(或糖炭)的混合物,将舟放进一个一端封闭的磨口高铝质制瓷管,此管与真空泵相联接,并以钼丝炉加热。
加热CaCN2或CaCN2与C的混合物须分两步进行:步在高真空中加热至1100~1150℃ 2~3h,使CaCN2充分分解,尽量将N2抽掉。此时应注意控制温度不要超过1150℃,以免在1170℃时形成CaCN2CaC2的低共熔物。第二步继续升温至1350℃ 1h,将剩余的N2除掉,得到纯白色碳化钙。纯度达到99%。
附氰氨基化钙的制法。纯的HCN经CaCl2和P2O5干燥后冷凝在低温接受器中,收集量要等于计算量的3倍。将CaCO3装在瓷舟里,瓷舟放在瓷管中,将瓷管加热到700~850℃。再将HCN的接受器温热至18℃。用夹杂着少量NH3的N2气携带HCN通过CaCO3,3h后可得到纯白色的CaCN2,其纯度为99.4%。
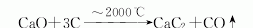
用途
1.电石用于化工生产约占60%,其余40%用于金属焊接和切割。以电石为原料可以生产一系列化工产品,如PVC树脂、聚乙烯醇、乙烯、氯丁橡胶、丁醇、辛醇、三氰乙烯、四氰乙烯、乙醛、乙炔炭黑、石灰氮等。而用量大的是生产PVC树脂,占化工用电石消费量的60%。电石粉末有刺激性,能损伤皮肤和呼吸系统。
2.是重要的基本化工原料,主要用于产生乙炔气、氰氨化钙。也用于有机合成等。[13]